Cobalto
Cobalto
Tecnológico, bonito e crucial para nossa saúde. Conheça o cobalto

O cobalto é conhecido e utilizado por suas propriedades de colorir e formar bonitos pigmentos azuis desde pelo menos 2.500 a.C. As pinturas azuis egípcias e os colares de óxido de cobalto da Prússia têm milhares de anos; vidros com cobalto foram encontrados num vaso grego datado de 100 a.C. O cobalto também foi usado para colorir o vidro na dinastia chinesa Tang, a partir de 618 d.C. Até o início do século 20 as pessoas exploraram o cobalto apenas por sua bonita cor, mas as coisas mudaram muito a partir dali. [1]
Atualmente, ele é reconhecido como um metal que permite o uso das novas tecnologias que exigem características como capacidade de armazenar energia, resistência a altas temperaturas, dureza, eficiência de processos e benefícios ambientais. [2]
Minérios – O cobalto é um metal prateado brilhante que pertence ao grupo dos metais de transição, ele é um dos 3 elementos de transição ferromagnéticos, junto com o ferro e o níquel. Seu símbolo é Co e seu número atômico é 27. É um metal muito duro e resistente, e seu ponto de fusão é altíssimo. Ele permanece magnético até mesmo quando submetido a altas temperaturas. [3]

Embora seja amplamente distribuído pelo planeta, o cobalto é apenas o trigésimo elemento em ordem de abundância. Mais de 200 minérios contêm cobalto, mas poucos são comercialmente viáveis. Os mais importantes são arsenetos e sulfetos, como esmaltita (CoAs2), cobaltita (CoAsS) e linaeita (Co3S4). Eles são quase sempre associados com níquel e, frequentemente, com cobre e chumbo; o cobalto é, normalmente, obtido como subproduto na recuperação desses metais. [4]
Em 2022, os maiores produtores de cobalto no mundo foram Congo, responsável por 70% da produção mundial, Indonésia, Rússia e Canadá. De acordo com o Departamento de Geologia dos Estados Unidos, a produção mundial do metal naquele ano foi de 190 mil toneladas. Existem apenas duas minas do mundo em que o cobalto é o principal produto, uma localizada no Marrocos e outra no estado norte-americano de Idaho. [5]
No Brasil, a única mina que produz cobalto, localizada em Niquelândia, Goiás, parou de operar em 2016, mas mesmo assim, em 2017 foram trabalhadas 150 mil toneladas de minérios estocados. Desses minérios foram obtidas 46 toneladas de cobalto refinado, segundo o Sumário Mineral Brasileiro de 2018. [6]
Aplicações – A maior parte do cobalto produzida atualmente – cerca de 57% – vai para a produção de baterias para veículos elétricos e para dispositivos eletrônicos, como tablets e smartfones. Ele também é usado como componente de circuitos e em semicondutores de computadores e telefones celulares. [2]
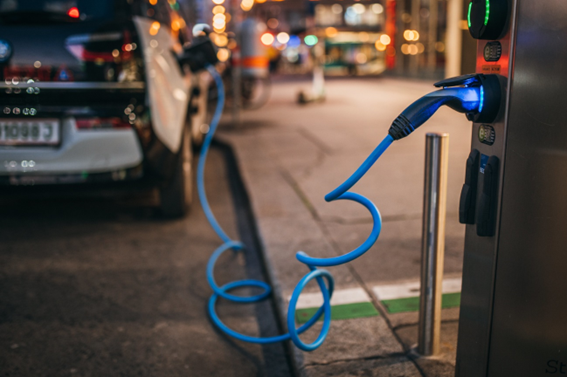
O cobalto é usado também para formar ligas. A Alnico, uma liga que consiste em alumínio, níquel e cobalto, é utilizada para fazer poderosos ímãs permanentes. Outras ligas que contêm cobalto, crômio e tungstênio são usadas para a fabricação de ferramentas de corte que suportam elevadas temperaturas. O cobalto também é usado para a fabricação de ligas usadas em motores de jatos e turbinas, em aços magnéticos e em alguns tipos de aços inoxidáveis. O metal é utilizado ainda em revestimento para conferir aos objetos uma superfície lisa que resiste à oxidação. [3]
Na indústria petroquímica, as propriedades únicas do cobalto tornam este elemento essencial nos catalisadores para remover enxofre, óxido nitroso e outras impurezas do petróleo bruto, o que confere melhor qualidade ao combustível e reduz as emissões de gases de efeito estufa. [2]
Há muito tempo o óxido de cobalto é usado como pigmento azul na indústria de cerâmica, e também para fabricar vidro azul. Atualmente, apenas 6% do cobalto produzido no mundo é utilizado para a fabricação de pigmentos para as indústrias de cerâmica, vidro e tintas. [2]
Graças às suas propriedades magnéticas, o cobalto é usado em uma série de aplicações, como sensores, acionadores e imagens de ressonância magnética. Ele também é usado em outras aplicações médicas, incluindo radioterapia, próteses para quadril e joelho e implantes dentários. [2]
Cobalto em humanos, plantas e animais – O cobalto é um metal essencial à vida em quantidades traço. Ele é o metal que está no centro da vitamina B12, que ajuda a regular o desenvolvimento das células e, portanto, do DNA e da produção de energia no corpo. [1]
Precisamos de quantidades muito pequenas de cobalto, e o corpo contém apenas 1 miligrama dele, aproximadamente. Os seres humanos ingerem cobalto ao beber água e ao consumir laticínios e carne. Em grandes doses o cobalto é carcinogênico. [1,2]

Animais recebem baixos níveis de cobalto por meio das plantas e da água. Bactérias no estômago de animais ruminantes requerem cobalto e, por sua vez, usam o cobalto para a síntese de vitamina B12. Esta vitamina também é essencial para a saúde dos rebanhos, e a deficiência de cobalto em animais nas fazendas é eliminada ao se adicionar cobalto aos fertilizantes do solo e à alimentação animal. [2]
O cobalto existente no solo é retirado por certas bactérias existentes nas raízes das plantas. Ali nas raízes o cobalto é usado para fornecer macronutrientes, ou compostos que contêm nitrogênio, necessário para as plantas. [2]
Nobel de Química – Em 2019, a Fundação Nobel concedeu o Prêmio Nobel de Química a três cientistas que desenvolveram ao longo de décadas a tecnologia das baterias de íons de lítio, que utilizam óxido de cobalto como um cátodo. Foram premiados os químicos Michael Stanley Whittingham, da Universidade Estadual de Nova York, e Akira Yoshino, da Universidade de Nagoya, no Japão, e o físico John Bannister Goodenough, da Universidade do Texas. As baterias de íons de lítio entraram no mercado em 1991 e revolucionaram o mundo: permitiram o desenvolvimento de aparelhos eletrônicos e, de acordo com a Fundação Nobel, abriram caminho para um mundo sem fios e livre de combustíveis fósseis. [7]
O cobalto também esteve presente no trabalho de outra importante pesquisadora. A química britânica nascida no Cairo, Dorothy Crowfoot Hodgkin, ganhou o Nobel de Química em 1964 por determinar as estruturas de importantes substâncias bioquímicas, como a penicilina, a insulina e a vitamina B12, que contém cobalto. Hodgkin foi a terceira mulher a ganhar um Prêmio Nobel, depois de Marie Curie e Irène Joliot-Curie. [8]
Duendes e vapores – O cobalto foi descoberto pelo químico sueco Georg Brandt. Em 1735 Brandt isolou um metal muito impuro, ou “regulus”, ao qual denominou “cobalto rex”. Em 1780 Torben Bergman mostrou que aquele era um novo elemento. [4]

Fonte: Wikimedia Commons
O nome do cobalto tem semelhança com a palavra grega cobalos, que significa mina, mas, provavelmente, é derivado da palavra germânica kobold, que significa duende ou espírito maligno, causador de problemas. Os mineiros dos países do norte europeu pensavam que a malícia daqueles duendes habitantes das minas era responsável por minérios que, quando fundidos, não forneciam os metais esperados e, para piorar, produziam vapores de arsênico altamente tóxicos (As4O6), o que tornava muito perigoso o trabalho de mineração. [4,2]
Referências
1- Cobalt2. Disponível em https://www.rsc.org/periodic-table/element/27/cobalt. Acesso em 30/05/2023.
2-Essential Cobalt. Disponível em https://www.cobaltinstitute.org/essential-cobalt-2/. Acesso em 31/05/2023.
3-The Element Cobalt. Disponível em https://education.jlab.org/itselemental/ele027.html. Acesso em 30/05/2023.
4-Greenwood, N., & Earnshaw, A. (1997). Chemistry of the Elements. Oxford: Butterworth-Heinemann.
5-Cobalt. Disponível em https://pubs.usgs.gov/periodicals/mcs2023/mcs2023-cobalt.pdf. Acesso em 15/06/2023.
6-Sumário Mineral. Disponível em https://www.gov.br/anm/pt-br/centrais-de-conteudo/publicacoes/serie-estatisticas-e-economia-mineral/sumario-mineral/pasta-sumario-brasileiro-mineral-2018/cobalto. Acesso em 04/07/2023.
7-Prêmio Nobel de Química de 2019. Disponível em https://www.nobelprize.org/prizes/chemistry/2019/press-release/. Acesso em 31/05/2023.
8-Dorothy Crowfoot Hodgkin. Disponível em https://www.sciencehistory.org/historical-profile/dorothy-crowfoot-hodgkin. Acesso em 31/05/2023.
Texto produzido pela jornalista Mari Menda da Gerência de Relações Institucionais
do CRQ-SP sob a supervisão de Sandra Helena Cruz, do Laboratório de
Biotecnologia de Alimentos e Bebidas da Escola Superior de Agricultura Luiz de Queiroz (ESALQ/USP)
Publicado em 20/02/2024


