Polônio
Polônio
Descoberto por Marie e Pierre Curie

O polônio, elemento de número atômico 84, foi descoberto em 1898 e recebeu o nome da Polônia, terra natal da química Marie Sklodowska Curie. Ela fez a descoberta do elemento juntamente com o marido Pierre Curie, em Paris. A lealdade de Marie Curie à terra natal foi uma provocação política; a Polônia não existia oficialmente à época, já que seu território estava ocupado pelos países vizinhos, Rússia, Prússia e Áustria. [1,2]
Os Curie isolaram o polônio a partir da pechblenda (óxido de urânio, U3O8), um material que contém urânio. Depois de muitos experimentos, Marie Curie observou que a pechblenda restante após a retirada do urânio era mais radioativa que o próprio urânio extraído dela, e suspeitou que aquele material deveria conter outro elemento radioativo. Curie teve que refinar manualmente por meses grandes quantidades de pechblenda para obter uma minúscula amostra de polônio e rádio, outro elemento radioativo descoberto por ela. Uma tonelada de minério de urânio contém apenas 100 microgramas (0,0001 gramas) de polônio. Por sua descoberta, o casal Curie e Henri Becquerel, que descobriu a radiação do urânio, dividiram o Prêmio Nobel de Física em 1903. [3,1]
A existência do polônio foi prevista por Mendeleev, que em sua tabela periódica pressupôs que deveria haver um elemento depois do bismuto, e antecipou que ele deveria ter peso atômico de 212. Os Curie extraíram o isótopo polônio-209 que tem meia-vida de 103 anos. [1]
Marie Curie morreu em 1934, vítima de uma leucemia, em decorrência de toda a exposição à radiação a que foi submetida durante sua carreira científica e acadêmica. Clique aqui para saber mais sobre Marie Curie e a visita que ela fez ao Brasil.
Antes de 1944 muito pouco polônio foi isolado. Isso mudou com o início do Projeto Manhattan, nos Estados Unidos, para desenvolvimento da bomba atômica. O polônio, um emissor de partículas alfa, e o berílio, que absorve as partículas alfa e emite nêutrons, foram usados como gatilhos para as primeiras bombas atômicas. Os dois elementos eram mantidos separados até o último momento, já que quando eram misturados eles desencadeavam a explosão. [2]
Assista ao vídeo sobre o polônio, produzido pela Universidade de Nottingham e legendado pelo Prof. Luís Brudna.
O polônio é um metal cinza prateado e radioativo. Ele está no grupo 16 da tabela periódica, o dos calcogênios, e seu símbolo é Po. O polônio ocorre em concentrações extremamente baixas na superfície da terra. Ele é altamente instável e todos os isótopos são radioativos. [1,2]
Sua posição na tabela periódica poderia fazê-lo um metal, um metaloide ou um não-metal, mas o polônio é classificado como metal porque sua condutividade elétrica diminui quando a temperatura aumenta. Por causa dessa propriedade, ele é usado para eliminar a eletricidade estática em máquinas de processos industriais que envolvem a rolagem de papel, fios ou folhas de metal, embora outros materiais também sejam usados com mais frequência para esse fim. O polônio é empregado ainda em pincéis para remover a poeira de filmes fotográficos e lentes, mas para isso o elemento deve estar cuidadosamente selado para proteger o usuário da contaminação. Um único grama de polônio atinge a temperatura de 500°C como resultado da radiação alfa que emite. Isto o torna útil como fonte de calor para equipamentos espaciais. Ele pode ser misturado ou adicionado a uma liga com berílio para fornecer uma fonte de nêutrons. [1,3]
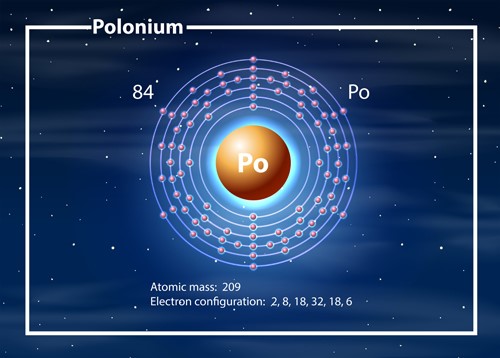
Como o polônio natural é muito raro, ele é produzido a partir do bismuto, também encontrado na pechblenda. Devido à sua escassez, o polônio é usualmente produzido pelo bombardeio de bismuto-209 com nêutrons dentro de um reator nuclear. Isto forma bismuto-210, que tem meia-vida de 5 dias. O bismuto-210 decai em polônio-210 através do decaimento beta. O polônio-210 tem meia-vida de 138,39 dias. [1,3]
O isótopo mais estável de polônio, polônio-209, tem meia-vida de 102 anos. Ele decai em chumbo-205 através do decaimento alfa. O polônio-209 pode ser obtido nos Estados Unidos, ao custo de 3.200 dólares por microcurie. Microcurie é a unidade de atividade radioativa; Curie (Ci) é a unidade que expressa 3,7 x 1010 desintegrações por segundo. Todo o polônio comercialmente produzido no mundo é fabricado na Rússia. [1,3]

O polônio é a peça-chave de um misterioso caso de envenenamento ocorrido em novembro de 2006 na Inglaterra. O ex-agente da inteligência russa Alexander Litvinenko, que desertara para o Ocidente e vivia na Inglaterra desde o ano 2000, morreu envenenado por polônio-210, um composto radioativo mortal. Ele ficou 22 dias hospitalizado. O chá que ele bebeu ao se encontrar em um hotel de Londres com dois ex-agentes russos estava envenenado, segundo as investigações. Litvinenko recebeu 10 microgramas de polônio, ou 10 milionésimos de grama, uma quantidade enorme e muito maior que a dose de 10 nanogramas, ou 10 bilionésimos de grama, já considerada fatal. O governo inglês e, posteriormente, a Corte Europeia de Direitos Humanos, responsabilizaram o Kremlin pelo assassinato de Litvinenko. A Rússia sempre negou envolvimento no crime. [5,6,4]
Cigarros – Materiais radioativos, como polônio-210 e chumbo-210, são encontrados naturalmente no solo e no ar. Eles também são encontrados nos fertilizantes altamente fosfatados usados pelos agricultores em suas lavouras. O polônio-210 e o chumbo-210 são absorvidos pelas folhas de tabaco e continuam nelas mesmo depois que o tabaco é processado. [7]
Quando um fumante acende um cigarro e inala a fumaça do tabaco, as substâncias tóxicas e radioativas da fumaça entram nos pulmões, onde podem causar danos diretos e imediatos às células e tecidos. As mesmas substâncias tóxicas e radioativas também podem prejudicar os pulmões das pessoas próximas. [7]
O polônio-210 se acumula por décadas nos pulmões dos fumantes. O alcatrão pegajoso do tabaco se acumula nas diminutas passagens de ar dos pulmões, ou bronquíolos, e as substâncias radioativas ficam presas. Ao longo do tempo essas substâncias podem levar ao câncer de pulmão. [7]
Referências
[1] – Polônio. Disponível em https://www.rsc.org/periodic-table/element/84/polonium. Acesso em 26/07/2022.
[2] – Six Secrets of Polonium. Disponível em https://www.smithsonianmag.com/science-nature/six-secrets-of-polonium-94821613/. Acesso em 05/08/2022.
[3] – Polonium. Disponível em https://education.jlab.org/itselemental/ele084.html. Acesso em 26/07/2022.
[4] – Gray, T. Os elementos. Ed. Edgard Blucher, 2011.
[5] – Russia Fatally Poisoned a Prominent Defector In London, A Court Concludes. Disponível em https://www.npr.org/2021/09/21/1039224996/russia-alexander-litvinenko-european-court-human-rights-putin. Acesso em 28/07/2022.
[6] – Alexander Litvinenko: Profile of murdered Russian spy. Disponível em https://www.bbc.com/news/uk-19647226. Acesso em 28/07/2022.
[7] – Centers for Disease Control and Prevention: Cigarette Smoking and Radiation. Acesso em 29/07/2022.
ATENÇÃO! Os experimentos com substâncias químicas mostrados nos vídeos aqui incluídos só devem ser reproduzidos na presença de um profissional ou professor de química, e em ambiente controlado. Não tente reproduzir esses experimentos por conta própria.
Texto produzido pela jornalista Mari Menda da Gerência de Relações Institucionais
do CRQ-SP sob orientação
técnica de Marta Eliza Bérgamo, do Centro de Educação Tecnológica da Fundação Indaiatubana de Educação e Cultura – FIEC.
Publicado em 04/01/2023


